Conceitos Atômico-Moleculares: Uma Visão Geral
Conceitos E Cálculos Das Leis E Da Teoria Atômico-Molecular Exemplos – E aí, meus queridos estudantes de Química! Vamos mergulhar no mundo fascinante dos átomos e moléculas, desvendando seus segredos com a vibe mais Makassar que você já viu. Preparem os cadernos e a caneta, porque a gente vai destrinchar tudo, desde os modelos atômicos até a geometria molecular, sem enrolação!
Evolução Histórica dos Modelos Atômicos
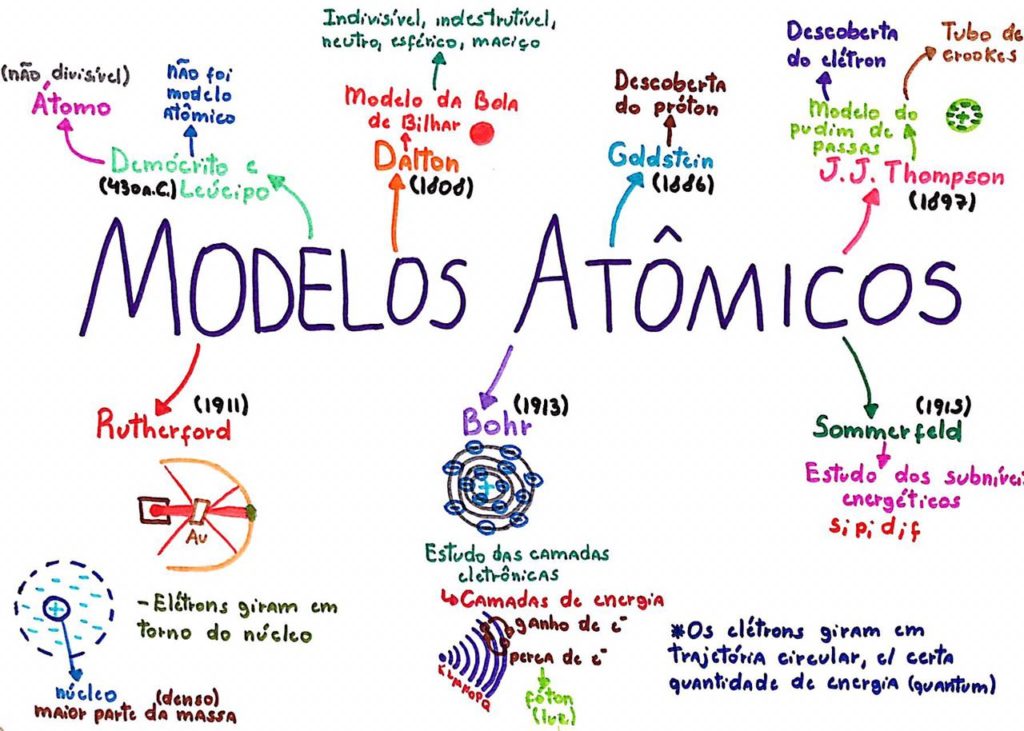
A jornada para entender a estrutura da matéria foi longa e cheia de reviravoltas, tipo novela mexicana! Começou com Dalton e sua ideia de átomos indivisíveis, bola de bilhar, saca? Depois veio Thomson com o pudim de passas, onde os elétrons estavam “espalhados” dentro de uma massa positiva. Rutherford, então, mudou o jogo com seu modelo planetário, com o núcleo positivo e os elétrons orbitando ao redor, parecido com o nosso sistema solar.
Mas esse modelo tinha seus problemas, e aí entrou Bohr, refinando a ideia com níveis de energia quantizados para os elétrons. Finalmente, o modelo quântico, mais complexo e sofisticado, descreve a probabilidade de encontrar um elétron em uma região específica do átomo, uma verdadeira viagem quântica!
Postulados da Teoria Atômico-Molecular
A teoria atômico-molecular, base de tudo isso, resume-se em alguns pontos chave: a matéria é feita de átomos; átomos de um mesmo elemento são idênticos; átomos podem se combinar para formar moléculas; reações químicas envolvem a reorganização de átomos. Simples assim, mas com implicações gigantescas!
Comparação entre os Modelos Atômicos de Bohr e Rutherford, Conceitos E Cálculos Das Leis E Da Teoria Atômico-Molecular Exemplos
Bohr melhorou o modelo de Rutherford ao introduzir a ideia de órbitas específicas para os elétrons, com níveis de energia quantizados. Rutherford, por sua vez, descreveu o átomo com um núcleo denso e positivo, mas não explicou como os elétrons se mantinham em órbita sem cair no núcleo. Ambos foram importantes, mas o modelo de Bohr foi um passo crucial para a compreensão da estrutura atômica.
Massa Atômica e Número Atômico: A Identidade do Átomo
Para entender a individualidade de cada átomo, precisamos conhecer dois números mágicos: a massa atômica e o número atômico. Vamos lá!
Definição de Massa Atômica e Número Atômico
O número atômico (Z) representa a quantidade de prótons no núcleo de um átomo, definindo o elemento químico. Já a massa atômica (A) é a soma do número de prótons e nêutrons no núcleo. Como os átomos de um mesmo elemento podem ter quantidades diferentes de nêutrons (isótopos), a massa atômica é uma média ponderada das massas isotópicas.
Cálculo da Massa Atômica Média
Vamos calcular a massa atômica média do cloro (Cl), que possui dois isótopos principais: 35Cl e 37Cl.
| Isótopo | Massa Isotópica (u) | Abundância (%) | Contribuição para a Massa Atômica Média (u) |
|---|---|---|---|
| 35Cl | 34.97 | 75.77 | 26.40 |
| 37Cl | 36.97 | 24.23 | 8.96 |
Massa atômica média do Cl = 26.40 + 8.96 = 35.36 u
Diferença entre Átomo, Íon e Molécula
Átomo é a unidade fundamental da matéria, íon é um átomo que ganhou ou perdeu elétrons, e molécula é um grupo de dois ou mais átomos ligados quimicamente.
Mol e Número de Avogadro: Contando Átomos e Moléculas
Imagine precisar contar todos os átomos em um grão de areia… impossível, né? É aí que entra o mol e o Número de Avogadro, facilitando nossa vida na contagem de átomos e moléculas.
Definição de Mol e Número de Avogadro
Um mol é a quantidade de uma substância que contém o mesmo número de entidades elementares (átomos, moléculas, íons etc.) que há átomos em 12 gramas de carbono-12. Esse número é o Número de Avogadro (N A), aproximadamente 6,022 x 10 23.
Conversão entre Gramas e Mols
Para converter gramas em mols, dividimos a massa em gramas pela massa molar da substância (massa atômica ou molecular em gramas/mol). Para converter mols em gramas, multiplicamos o número de mols pela massa molar.
Exemplo: Quantos mols há em 10g de água (H 2O)? Massa molar da H 2O = 18 g/mol. Número de mols = 10g / 18 g/mol ≈ 0.56 mols.
Cálculo do Número de Átomos ou Moléculas
Para calcular o número de átomos ou moléculas, multiplicamos o número de mols pelo Número de Avogadro.
Fórmulas Químicas e Estequiometria: As Receitas da Química: Conceitos E Cálculos Das Leis E Da Teoria Atômico-Molecular Exemplos
A estequiometria é a parte da química que estuda as relações quantitativas entre reagentes e produtos em uma reação química. É como a receita de bolo da química, precisamos das quantidades certas para obter o resultado desejado.
Determinação da Fórmula Empírica e Molecular
A fórmula empírica mostra a proporção mais simples dos átomos em um composto, enquanto a fórmula molecular mostra o número real de átomos de cada elemento na molécula.
Cálculo da Porcentagem em Massa
Para calcular a porcentagem em massa de um elemento em um composto, dividimos a massa do elemento pela massa total do composto e multiplicamos por 100.
Resolução de Problemas de Estequiometria
Vamos resolver um problema de estequiometria passo a passo. Considere a reação balanceada: 2H 2 + O 2 → 2H 2O. Se temos 4g de H 2 e excesso de O 2, quantos gramas de H 2O são produzidos?
- Calcular os mols de H2: 4g / 2g/mol = 2 mols
- Usar a proporção estequiométrica para encontrar os mols de H 2O: 2 mols H 2 x (2 mols H 2O / 2 mols H 2) = 2 mols H 2O
- Calcular a massa de H 2O: 2 mols H 2O x 18g/mol = 36g H 2O
Ligações Químicas: Unindo os Átomos
As ligações químicas são as forças que unem os átomos, formando moléculas e compostos. Existem diferentes tipos de ligações, cada uma com suas características.
Tipos de Ligações Químicas
As principais ligações químicas são: iônica (transferência de elétrons), covalente (compartilhamento de elétrons) e metálica (nuvem de elétrons deslocalizados).
Propriedades Físicas de Compostos
| Tipo de Ligação | Ponto de Fusão | Condutividade Elétrica | Solubilidade em Água |
|---|---|---|---|
| Iônica | Geralmente alto | Só em solução aquosa ou fundida | Muitos são solúveis |
| Covalente | Variável | Geralmente baixa | Variável |
| Metálica | Variável | Alta | Geralmente insolúvel |
Estruturas de Lewis
As estruturas de Lewis representam a distribuição dos elétrons de valência em uma molécula, mostrando os pares de elétrons compartilhados e não compartilhados. Por exemplo, a molécula de água (H 2O) possui dois pares de elétrons compartilhados entre o oxigênio e cada hidrogênio, e dois pares de elétrons não compartilhados no oxigênio.
Geometria Molecular e Teoria VSEPR: A Forma das Moléculas
A geometria molecular descreve a disposição espacial dos átomos em uma molécula, influenciando suas propriedades. A Teoria VSEPR (Valence Shell Electron Pair Repulsion) ajuda a prever essa geometria.
Teoria VSEPR

A Teoria VSEPR afirma que os pares de elétrons ao redor do átomo central se repelem e se posicionam o mais afastados possível, determinando a geometria molecular. Por exemplo, a molécula de metano (CH 4) tem geometria tetraédrica, com os quatro átomos de hidrogênio nos vértices de um tetraedro.
Previsão da Geometria Molecular
A molécula de água (H 2O) tem geometria angular devido aos dois pares de elétrons não compartilhados no oxigênio. Já o dióxido de carbono (CO 2) tem geometria linear, pois não possui pares de elétrons não compartilhados no carbono.
Diagramas de Geometria Molecular
Para a molécula de água, imagine um átomo de oxigênio no centro, com dois átomos de hidrogênio ligados a ele formando um ângulo de aproximadamente 104.5°. Os dois pares de elétrons não ligantes do oxigênio também influenciam a geometria, criando uma forma angular, não linear. Para o metano (CH 4), imagine um átomo de carbono no centro, com quatro átomos de hidrogênio ligados a ele em uma disposição tetraédrica, formando ângulos de 109.5° entre as ligações.
Gases Ideais e Lei dos Gases Ideais: O Comportamento dos Gases
Gases ideais são um modelo teórico que simplifica o comportamento de gases reais, facilitando os cálculos. A lei dos gases ideais relaciona pressão, volume, temperatura e número de mols de um gás ideal.
Lei dos Gases Ideais
A lei dos gases ideais é expressa pela equação: PV = nRT, onde P é a pressão, V é o volume, n é o número de mols, R é a constante dos gases ideais e T é a temperatura em Kelvin.
Resolução de Problemas
Exemplo: Qual o volume ocupado por 2 mols de um gás ideal a 25°C (298 K) e 1 atm de pressão? Usando a equação PV = nRT, e considerando R = 0.082 atm.L/mol.K, encontramos V ≈ 49 L.
Comparação entre Gases Reais e Ideais
Gases reais desviam do comportamento ideal em altas pressões e baixas temperaturas, onde as forças intermoleculares e o volume das moléculas tornam-se significativos. Em condições de baixa pressão e alta temperatura, o comportamento dos gases reais se aproxima do comportamento ideal.
Por que o modelo atômico de Bohr é considerado um modelo simplificado?
O modelo de Bohr, apesar de seu sucesso em explicar o espectro de emissão do hidrogênio, falha ao descrever átomos com mais de um elétron, não considerando a natureza ondulatória dos elétrons e a incerteza na sua posição e momento.
Quais são as principais limitações da lei dos gases ideais?
A lei dos gases ideais assume que as moléculas de gás não têm volume e não interagem entre si, o que não é verdade para gases reais, especialmente em altas pressões e baixas temperaturas.
Como a geometria molecular afeta as propriedades de uma substância?
A geometria molecular influencia diretamente a polaridade da molécula, afetando suas propriedades físicas como ponto de fusão, ponto de ebulição e solubilidade.

